 戲中人
查看知乎原文
戲中人
查看知乎原文
氰离子毒性来源于超强的配位能力,干扰细胞内辅助正常功能的金属离子,比如亚铁离子。一旦结合就难解离,在常温条件下异常稳定。
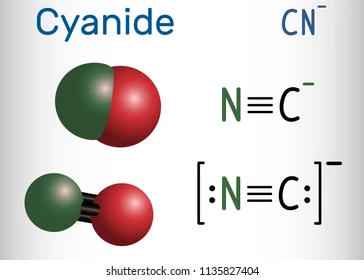
反应式
6CN- + Fe2+ = [Fe(CN-)6]4-
所以为什么亚铁氰化钾反而其实无毒,因为氰离子与亚铁离子配位了,没办法出来危害人间。
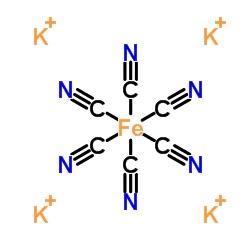
血红蛋白中有亚铁离子运输氧气,而线粒体上也需要铁硫蛋白载入的亚铁离子与铁离子的氧化还原变化传递电子,最终氧化磷酸化途径变成 atp 提供能量,铁被氰根绑定之后,整个呼吸链的线路都瘫了,结果就是细胞缺氧罢工状态,组织坏死,动物死亡。
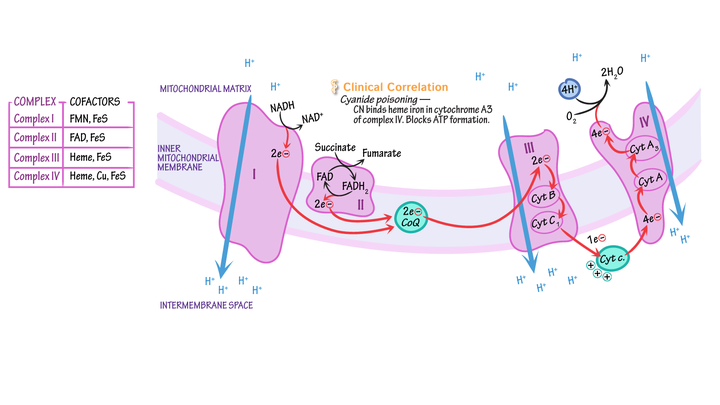
这个配位能力是因为氮元素和碳元素的偶极矩不平等造成非常大的极性和配位孤电子。与氰根有点类似的一氧化碳也能抢夺红细胞的亚铁离子配位,但是一氧化碳只是气体,浓度限制所以危害毒杀速度不如氰化物。
进化论上来说,因为动物选择了铁离子(亚铁)在氧化呼吸链的重要位置,而铁离子被氰根高效攻击捕获细胞当机,所以造成毒性。
为什么动物祖先要选铁离子在线粒体呼吸链氧化还原中的电子传递的媒介?常见的可变价的二价金属离子,比如锰 +2+3+4+6+7,理论上也可以。我推测还是早期海洋富铁造成的。
铁硫簇(铁硫蛋白)是普遍存在于生物体内的最古老的生命物质之一 1960 年人们对固氮细菌、亚线粒体片段及哺乳动物的起源进行研究时发现了一种具有高效氧化还原能力的蛋白质.后来被证明是铁硫蛋白.此后对铁硫簇的研究才得以迅速展开。铁硫蛋白结构中包含有铁与巯基丙氨酸中的硫结合成的具有一定构型的铁硫簇合物,基本结构单元主要以 Fe2S2、Fes、Fe4S4 这 3 种簇合物的形式而存在。